即可将网页分享至朋友圈
近日,自动化工程学院谢永乐教授“电磁与声波测量”团队与加拿大不列颠哥伦比亚大学(University of British Columbia, UBC)AI in Medicine实验室(AIM Lab)合作完成的医工结合研究成果 “KAFSTExp: Kernel Adaptive Filtering with Nyström Approximation for Predicting Spatial Gene Expression from Histology Image” 在线发表于国际著名期刊 IEEE Journal of Biomedical and Health Informatics(IEEE JBHI)。
该研究针对空间转录组数据获取成本高、数据稀缺、预测模型泛化性差等关键难题,提出了一种轻量级、高效且具有良好泛化能力的空间基因表达预测框架。该论文第一作者为2020级博士研究生刘浩然,通讯作者为电子科技大学的李西峰副教授和不列颠哥伦比亚大学的Ali Bashashati教授,共同作者还有谢永乐教授及Hossein Farahani博士,2023级博士研究生董文浩在论文的理论推导和实验过程中也提供了重要支持。
空间转录组(Spatial Transcriptomics, ST)技术能够在保留组织空间结构信息的同时,获取细胞或区域的基因表达谱,是解析肿瘤空间异质性、揭示疾病发生机制的重要手段。然而,ST实验依赖昂贵的测序平台和复杂的实验流程,难以在常规临床中大规模应用。相比之下,传统的H&E染色病理切片获取成本低、流程成熟。如果能从病理图像中精准预测基因表达,就能以极低成本获得空间组学信息,从而极大提升临床可及性和科研效率。但现有深度学习方法往往存在参数量大、易过拟合、对有限ST数据泛化性不足等问题,这成为制约技术落地的瓶颈。
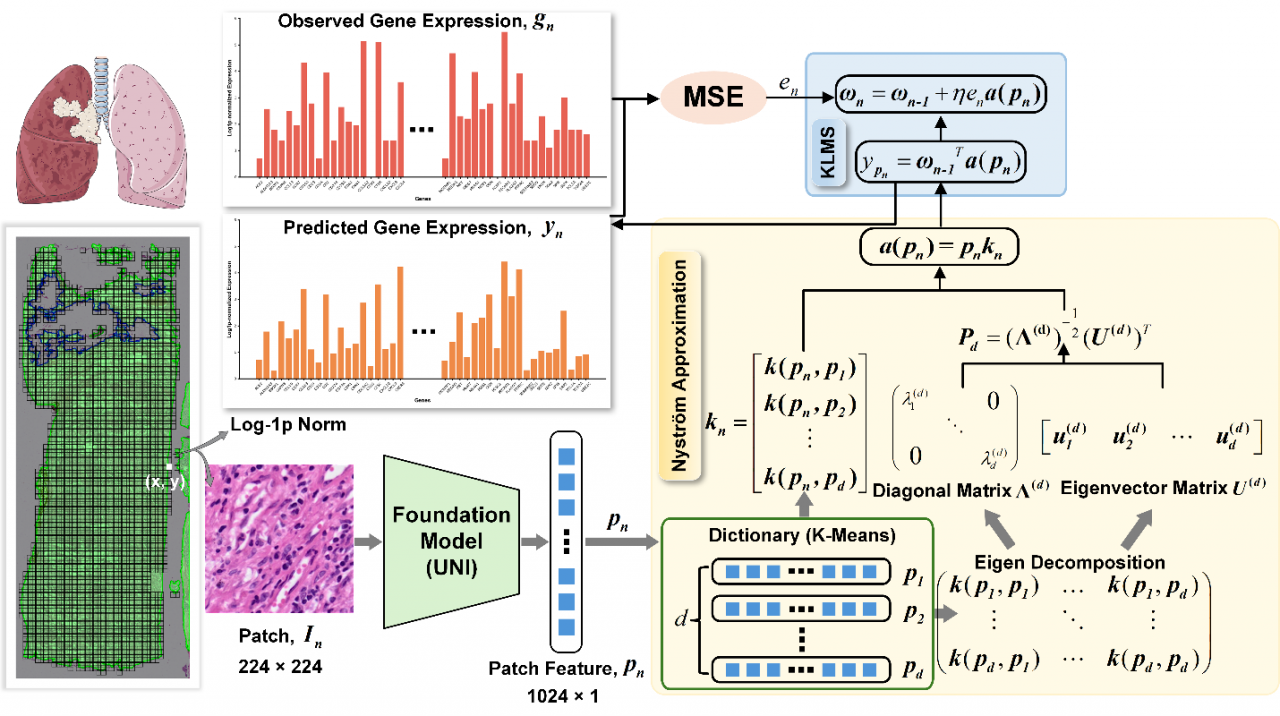
图1 KAFSTExp的总体结构框图
针对上述挑战,研究团队提出了KAFSTExp框架,将病理图像基础模型UNI与核自适应滤波(Kernel Adaptive Filtering, KAF)有机结合,并引入Nyström近似以实现模型稀疏化与计算加速。该方法充分发挥了病理基础模型在小样本场景下的高质量特征提取能力,以及KAF在处理非线性映射问题上的精确性与稳定性。通过Nyström近似,KAFSTExp在保持预测精度的同时,显著降低了计算复杂度和显存占用,使其在高分辨率大规模ST数据中依然高效可用。
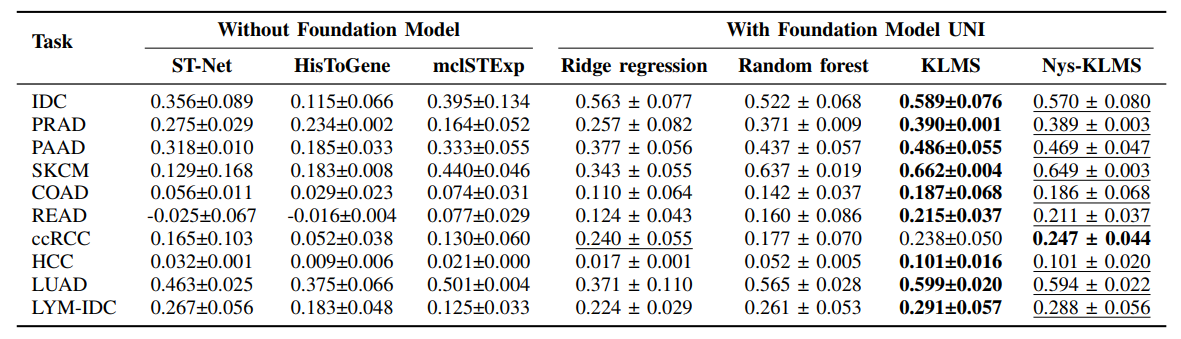
图2 KAFSTExp与现有方法在HEST-Benchmark上的性能对比
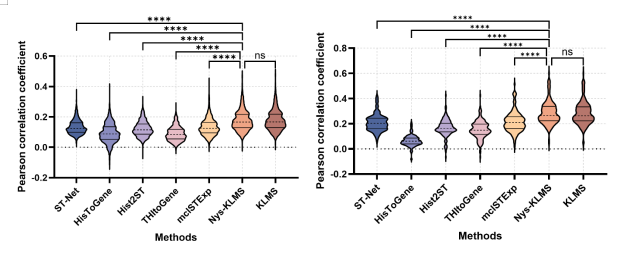
图3 KAFSTExp及现有方法在HER2+和cSCC数据集上的性能对比
在涵盖10种癌症类型的HEST-Benchmark数据集以及HER2+乳腺癌和皮肤鳞癌(cSCC)等多个经典ST数据集上的系统实验表明,KAFSTExp在预测精度上全面优于现有主流方法,平均皮尔森相关系数(PCC)相对提升值可达19.80%。对于临床高度关注的关键癌症相关基因,KAFSTExp同样表现出卓越的预测性能,显示其在肿瘤分子分型、预后评估以及个性化治疗策略制定中的潜在价值。外部独立验证结果进一步证明了该方法在跨平台、跨样本场景下的稳健性,为临床转化奠定了坚实基础。

图4 使用DAVID平台针对研究中涉及的目标基因进行的GO 和KEGG通路丰度分析结果
本研究展示了在无需RNA测序的前提下,仅通过常规H&E染色病理图像即可实现较高精度的空间基因表达预测,为空间组学研究和临床转化提供了更经济高效的替代路径,尤其适用于资源受限的医学场景。该工作不仅推动了计算病理与空间组学的交叉融合,也为未来在大规模临床应用中实现快速、低成本的分子信息获取奠定了基础。
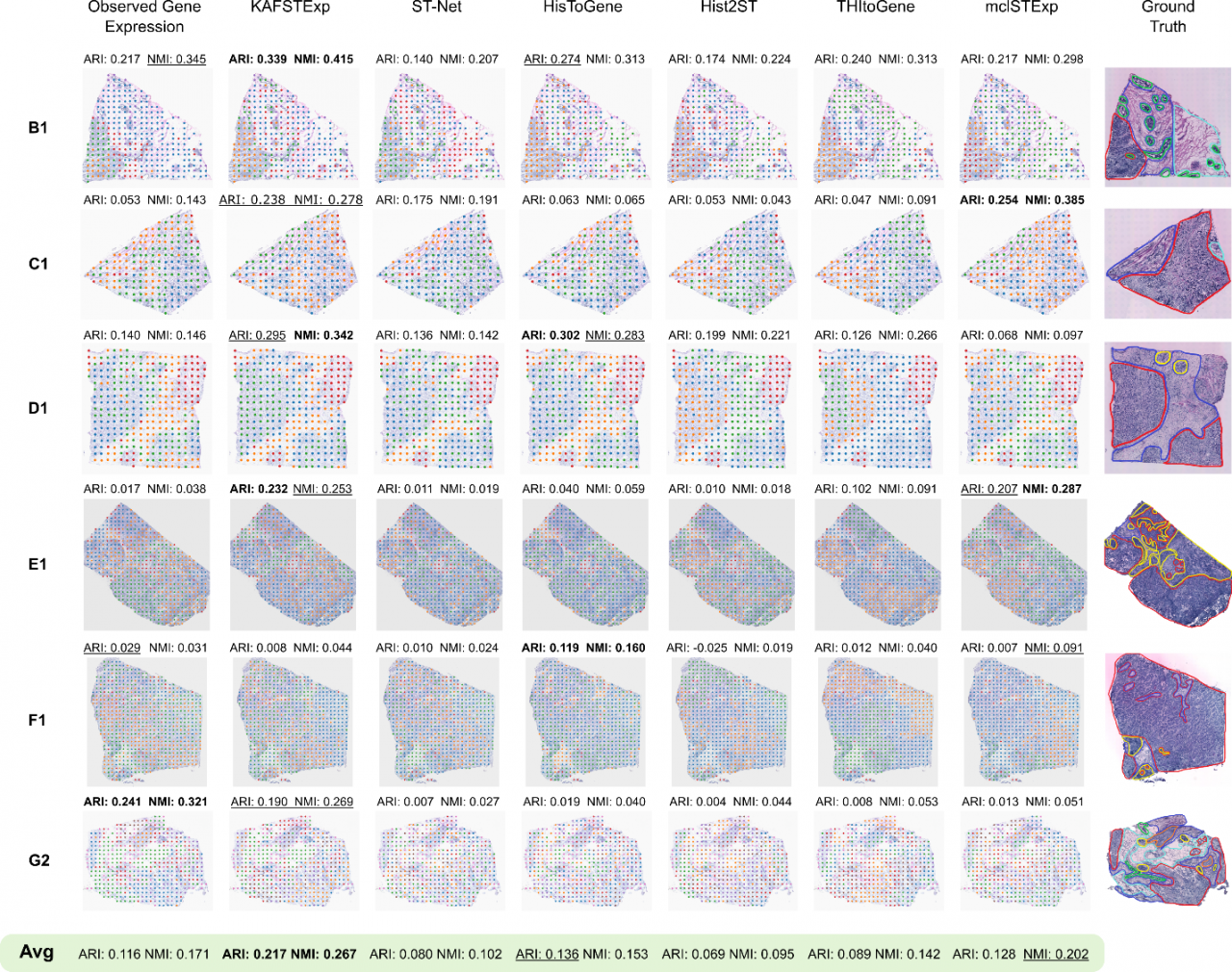
图5 组织空间区域检测结果图
该研究的海外合作单位AIM实验室隶属于 UBC 应用科学学院(Faculty of Applied Science)与医学院(Faculty of Medicine)联合设立的生物医学工程学院(School of Biomedical Engineering),是汇聚计算、工程与医学多学科力量的重要研究机构。AIM Lab聚焦开发可推广的AI模型,以提升组织病理图像分析的准确性和效率。
电子科技大学自动化工程学院“电磁与声波测量”团队,遵循习近平总书记“四个面向”之 “面向人民生命健康”,近年联合电子科技大学医学院、四川省人民医院肾内科的李贵森、邹玉蓉、张萍、彭雷等临床医生,在肾脏病的人工智能诊断方面也取得重要进展。
论文链接:https://ieeexplore.ieee.org/document/11112549
编辑:刘瑶 / 审核:王晓刚 / 发布:陈伟


