即可将网页分享至朋友圈
光学相干断层成像(Optical Coherence Tomography, OCT)作为一种非侵入、高分辨率的三维成像技术,已广泛应用于眼科、心血管、皮肤等医学临床领域。然而,受限于相干成像固有散斑等噪声干扰、生物组织复杂结构及三维图像处理等挑战,OCT在真实临床环境中应用仍面临诸多挑战。针对这一系列难题,电子科技大学光电科学与工程学院光电子器件与应用技术团队(负责人:刘永教授)医用光学课题组持续开展创新研究,围绕OCT三维成像及深度学习处理与临床转化应用取得了多项重要成果,相关研究成果近期连续发表于IEEE国际医学影像领域顶级期刊IEEE Transactions on Medical Imaging (2025年IF=9.8)。该系列工作中,电子科技大学均为唯一通讯单位,团队博士生吴壬熊、硕士生覃小洋和裴绍雨等为第一作者,倪光明副教授为通讯作者。
实现“无散斑”的光学相干层析成像 让图像更接近“真值”
在题为《Toward ground-truth optical coherence tomography via three-dimensional unsupervised deep learning processing and data》的研究中,团队提出了全新的三维无监督深度学习/三维数据自驱动无散斑OCT成像策略(tGT-OCT),如图1所示。该方法利用相干三维成像数据的空间相干属性,并结合三维无监督卷积网络,从OCT体数据中自动鉴别散斑等噪声与真实组织结构,首次在无需干净对照数据的情况下实现了强适应性的“真值级”(Ground truth)三维无散斑OCT成像。研究结果表明,该技术不仅显著提升了成像质量,还能解析出以往被散斑掩盖的微小结构,其成像效果接近目前公认的“理想物理方案”(Speckle-free OCT. Nature Methods 14, 767 (2017)),但无需复杂昂贵的光学装置,也不会牺牲成像灵敏度和时间分辨率。该方法有望推广到眼科视网膜疾病、心血管斑块检测及皮肤病诊断等多个临床场景,为临床医生提供更清晰、更可靠的“光学活检”。
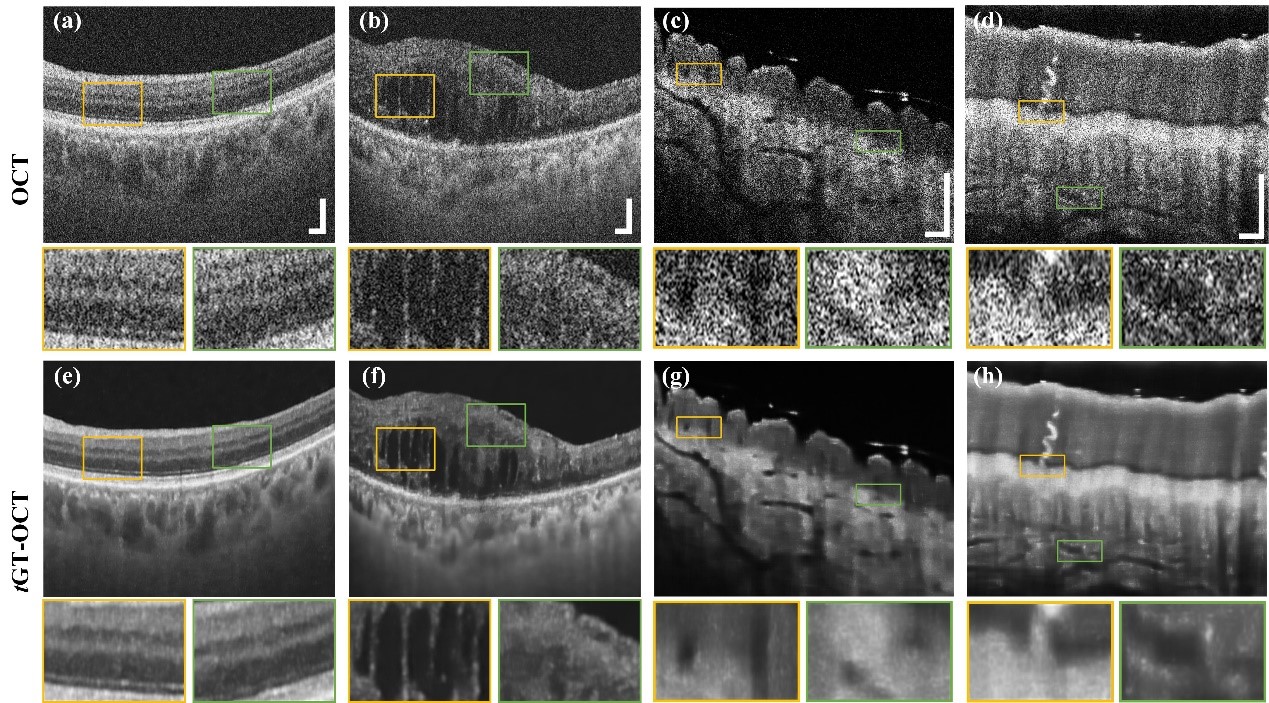
图1. 眼底视网膜(左)与人体皮肤(右)tGT-OCT无散斑成像
心脏支架植入的三维可视量化评估 助力精准PCI手术
支架植入是冠心病治疗的关键手段,但若支架与血管壁贴合不良,易引发再狭窄或血栓等风险。现有评估依赖医生逐帧观察X-ray或超声等二维图像,既耗时费力,也可能遗漏细节。在题为《3D distance-color-coded assessment of PCI stent apposition via deep-learning-based three-dimensional multi-object segmentation》研究中,团队首次提出了三维空间距离-颜色编码(3D DccA)PCI手术方法,图2所示。该方法基于心血管OCT三维内窥成像和混合维度(3D+2D)深度学习三维多目标分割,能够精准提取冠脉腔面与金属支架,并通过三维空间距离计算与颜色映射直观呈现支架贴壁度。研究表明,该方法在支架与腔面分割上精度超过95%,实现了PCI术后支架贴壁度的三维直观评估,有助于医生术中“一眼”识别潜在的贴壁异常和再狭窄风险,为个体化心血管PCI干预提供了全新智能化工具。
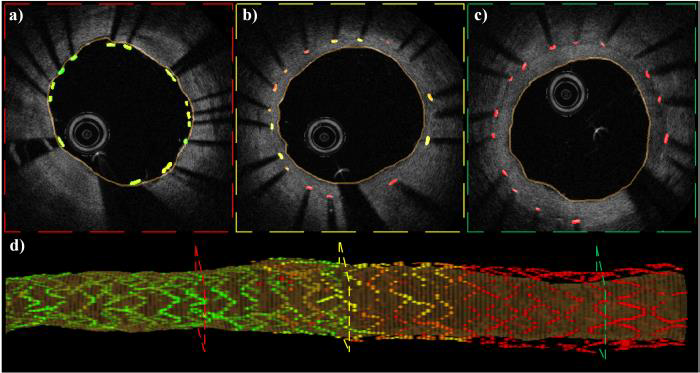
图2. 人体冠状动脉PCI植入支架3D DccA 三维可视化评估:术后内膜新生并发症
揭示汗腺随温度变化的三维形态学反应 无创观察人体“散热系统”
皮肤汗腺是人体调节体温的重要“散热装置”,也是多种皮肤疾病的病灶所在。在题为《3D deep-learning-based segmentation of human skin sweat glands and their 3D morphological response to temperature variations》研究中,团队基于前述工作研发的tGT-OCT无散斑成像和三维图像深度学习分割等技术,首次实现了在体汗腺三维形态无损获取与定量分析,图3所示。通过tGT-OCT获取高质量的人体皮肤3D图像并结合三维深度学习分割,研究定量揭示了人体汗腺三维螺旋结构及其在不同温度下的三维形态变化,例如在43℃相较10℃条件下汗腺体积、表面积和导管长度分别增加42.0%、26.4%和12.8%(p<0.001)。该研究为皮肤腺体功能评价及相关疾病诊断提供了实时、无创、可量化的新手段,推动了皮肤病学和生理学研究的深入发展。
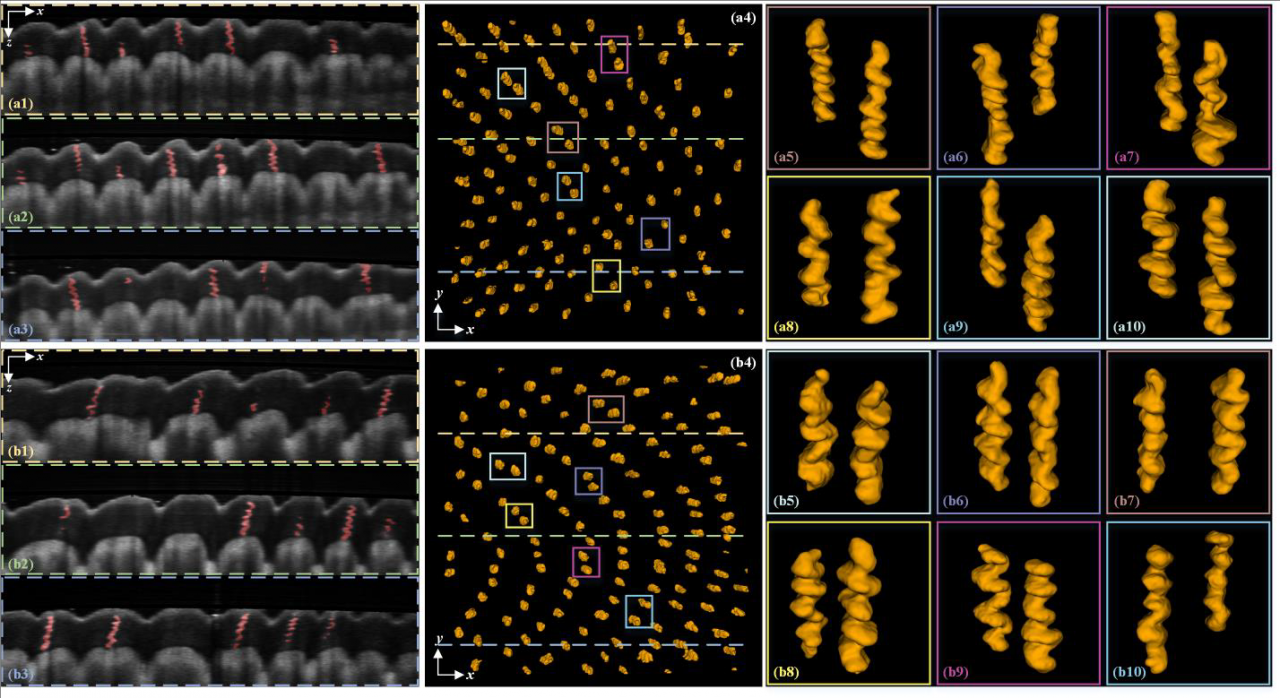
图3. 人体皮肤汗腺三维形貌:首次揭示汗腺三维螺旋形貌(上图为人手指处采样)
编辑:助理编辑 / 审核:王晓刚 / 发布:陈伟


